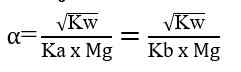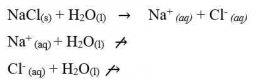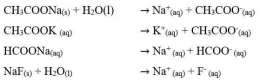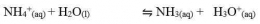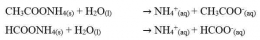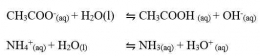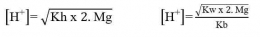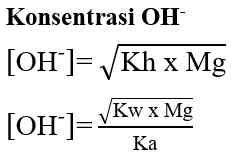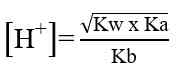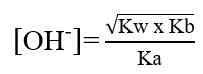Karena ion Na+ dan Cl- bersifat stabil di dalam air maka tidak terjadi reaksi dengan air karena masing-masing berasal dari asam kuat dan basa kuat, jadi melarutnya garam ini tidak merubah konsentarsi ion H+ dan ion OH-. Sehingga garam dengan tipe ini, pH-nya sama dengan pH air yaitu 7 (larutan bersifat netral).
2. Garam yang Berasal dari Asam Lemah dan Basa Kuat
Garam ini akan terionisasi sempurna dalam air dan akan menghasilkan ion-ion. Anion berasal dari asam lemah dan kation berasal dari basa kuat. Perhatikan reaksi-reaksi berikut.

Anion dari asam lemah CH3COO-, HCOO-, dan F- akan bereaksi dengan air (terhidrolisis) sesuai dengan persamaan reaksi berikut.

Ingat kembali sifat-sifat asam-basa Bronsted-Lowry. Basa konjugasi dari asam lemah merupakan basa yang relatif kuat dibandingkan basa konjugasi dari asam kuat sehingga dapat bereaksi dengan air. Adanya ion OH- dalam hasil reaksi menunjukkan bahwa larutan garam tersebut bersifat basa. Jika diuji dengan kertas lakmus merah, warna kertas lakmus akan berubah menjadi biru. Ion K+ dan Na+ yang berasal dari basa kuat tidak bereaksi dengan air, artinya tidak mengalami hidrolisis. Hidrolisis yang terjadi pada anion saja atau pada kation saja disebut hidrolisis parsial (hidrolisis sebagian). Jadi, garam jenis ini mengalami hidrolisis parsial.
3. Garam yang berasal dari Basa Lemah dan Asam Kuat
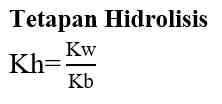
Garam ini akan terionisasi sempurna dalam air dan akan menghasilkan ion-ion. Kation berasal dari basa lemah dan anion berasal dari asam kuat. Perhatikan reaksi-reaksi hidrolisis berikut.

Kation dari basa lemah (NH4+) akan terhidrolisis dengan reaksi sebagai berikut.