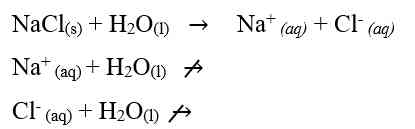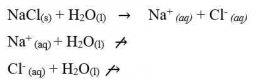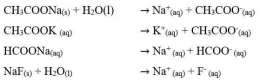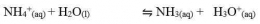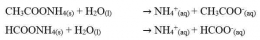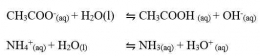Pernahkah Anda menggunakan garam dapur, soda kue dan pupuk ZA? Untuk apa bahan-bahan tersebut? Mungkin Anda menggunakan garam dapur untuk memberikan rasa asin pada makanan, soda kue untuk membuat adonan kue menjadi lebih mengembang dan pupuk ZA untuk menyuburkan tanaman.
Secara kimiawi Anda tentu sudah mengenal bahwa garam dapur, soda kue, dan pupuk ZA (Zwavelzure Ammoniak) adalah nama trivial, coba Anda telusuri bagaimana nama IUPAC nya? Berdasarkan nama IUPAC yang telah Anda telusuri, masih ingatkah Anda bagaimana rumus kimia dari bahan-bahan tersebut? Pada pembelajaran sebelumnya, Anda telah mempelajari tentang penggolongan senyawa, yakni: asam, basa, dan garam. Termasuk golongan senyawa manakah garam, soda kue dan pupuk Za? Seandainya Anda mengambil satu sendok pupuk ZA, (NH4)2SO4 kemudian Anda melarutkannya ke dalam air, apa yang terjadi? Apakah pupuk ZA larut? Apabila larutan diuji menggunakan kertas lakmus, maka perubahan apa yang terjadi pada kertas lakmus? Bagaimana sifat larutannya? Larutan senyawa garam jika diuji dengan menggunakan pH meter atau indikator universal menunjukkan pH larutan garam dengan kemungkinan yang berbeda-beda. Mengapa demikian? Untuk mempelajari lebih lanjut akan dikaji pada pokok bahasan Hidrolisis Garam.
Apabila larutan asam dicampur dengan larutan basa, maka secara spontan akan terjadi reaksi membentuk garam dan air.
Air terbentuk dari penggabungan ion H+ dari asam dan ion OH- dari basa. Karena air (H2O) bersifat netral, maka reaksi antara ion H+ dengan ion OH- disebut dengan reaksi penetralan. Sementara itu, kation dari asam selain OH- dan anion dari basa selain H+ akan membentuk garam.
Contoh:
HCl(aq) + NaOH(aq) --> NaCl(aq) + H2O(l)
Asam Basa Garam Air
Bagaimana dengan sifat garam yang terbentuk dari reaksi asam basa? Apakah semua garam yang terbentuk juga hanya bersifat netral? Faktanya ada garam yang bersifat asam, basa, maupun netral. Sifat senyawa asam dan basa dapat diidentifikasi dengan menggunakan indikator, salah satunya yaitu dengan menggunakan kertas lakmus. Untuk menjawab pertanyaan-pertanyaan tersebut, maka kita akan mempelajari tentang konsep hidrolisis garam.
Jenis-jenis Garam yang Terhidrolisis dalam Air
Sifat larutan garam dapat dijelaskan dengan konsep hidrolisis. Hidrolisis merupakan istilah yang umum digunakan untuk reaksi zat dengan air (hidrolisis berasal dari kata hydro yang berarti air dan lysis yang berarti peruraian). Menurut konsep ini komponen garam (kation dan anion) yang berasal dari asam lemah atau basa lemah bereaksi dengan air (terhidrolisis) membentuk H3O+ atau OH-. Hidrolisis kation menghasilkan ion H3O+ dan hidrolisis anion menghasilkan OH-.