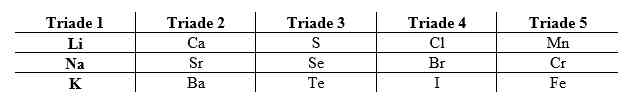
Kelemahan dari Tabel Periodik Mendeleev adalah sebagai berikut.
1) Apabila ditinjau dari bertambahnya massa atom relatif, ada beberapa urutan unsur yang terbalik.
2) Panjang periode tidak sama.
3) Dalam golongan VIII, dimasukkan triade besi (Fe, Co, dan Ni), triade platina ringan (Ru, Rh, dan Pd), dan triade platina (Os, Ir, dan Pt).
5. Sistem Periodik Unsur Modern
Henry G. J. Moseley pada tahun 1914 menemukan kesalahan dalam tabel periodik Mendeleev, yaitu unsur yang terbalik letaknya dan menemukan bahwa urutan unsur dalam tabel periodik sesuai dengan kenaikan nomor atom suatu unsur. Sistem periodik modern juga disebut sebagai sistem periodik bentuk panjang yang disusun berdasarkan kenaikan nomor atom dan kemiripan sifat. Sama seperti tabel periodik mendeleev, dalam sistem periodik modern terdapat periode dan golongan.
a. Penentuan Periode dalam Sistem Periodik Modern
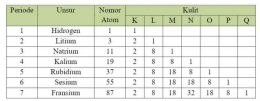
Dalam sistem periodik, periode ditempatkan pada lajur horizontal atau lajur mendatar. Periode menunjukkan suatu nomor kulit yang berisi elektron (n terbesar) yang didasarkan atas konfigurasi elektronnya. Terdapat 7 periode dalam sistem periodik modern, yaitu:
- Periode 1 merupakan periode sangat pendek yang berisi 2 unsur
- Periode 2 merupakan periode pendek yang berisi 8 unsur
- Periode 3 merupakan periode pendek yang berisi 8 unsur
- Periode 4 merupakan periode panjang yang berisi 18 unsur
- Periode 5 merupakan periode panjang yang berisi 18 unsur
- Periode 6 merupakan periode sangat panjang yang berisi 32 unsur, dimana pada periode ini terdapat unsur Lantanida yaitu nomor 58 sampai sampai nomor 71 yang letaknya dibagian bawah
- Periode 6 merupakan periode belum lengkap yang berisi 24 unsur, dimana pada periode ini terdapat deretan unsur Aktinida yaitu nomor 90 sampai sampai nomor 103 yang letaknya dibagian bawah
b. Penentuan Golongan dalam Sistem Periodik Modern
Dalam sistem periodik, golongan ditempatkan pada lajur vertikal atau lajur tegak. Unsur-unsur segolongan adalah unsur yang ada dalam satu lajur tegak, terdapat delapan golongan utama golongan utama dan delapan golongan transisi. Unsur-unsur golongan utama yaitu:
- Golongan IA disebut sebagai golongan alkali
- Golongan IIA disebut sebagai golongan alkali tanah
- Golongan IIIA disebut sebagai golongan boron
- Golongan IVA disebut sebagai golongan karbon
- Golongan VA disebut sebagai golongan nitrogen
- Golongan VIA disebut sebagai golongan oksigen
- Golongan VIIA disebut sebagai golongan halogen
- Golongan VIIIA disebut sebagai golongan gas mulia
Pada periode 6 dan 7 terdapat masing-masing 14 unsur yang disebut unsur-unsur transisi dalam yang mempunyai kemiripan sifat yaitu unsur-unsur lantinida dan aktinida. Kedua unsur tersebut disebut unsur-unsur transisi dalam, dimana unsur-unsur lantinida pada periode 6 golongan IIIB, dan unsur-unsur aktinida pada periode 7 golongan IIIB.