Penyakit kardiovaskular kerap menjadi ancaman utama bagi kesehatan global. Data kesehatan masyarakat yang ada di WHO menunjukkan bahwa pada tahun 2016 saja, penyakit kardiovaskular telah menyebabkan 17,9 juta kematian secara global dan diprediksikan meningkat menjadi sekitar 23,3 juta orang pada tahun 2030 [1]. Salah satu penyebab utama penyakit kardiovaskular adalah adanya pembentukan bekuan darah yang tidak diinginkan di dalam pembuluh darah. Kondisi ini kita kenal sebagai trombosis dalam istilah medis.
Antikoagulan dan antiplatelet telah lama digunakan untuk mengatasi penyakit kardiovaskular. Akan tetapi, kedua golongan obat ini tidak dapat melarutkan bekuan (trombus) yang ada. Oleh karena itu, agen fibrinolitik mulai mendapat banyak perhatian karena kemampuannya dalam melisiskan bekuan fibrin di dalam pembuluh darah [2].
Dalam beberapa dekade terakhir, banyak enzim fibrinolitik dari sumber daya alam, yang telah diidentifikasi dan dipelajari, seperti ular, cacing tanah, serangga, tanaman, jamur, mikroorganisme, dan makanan fermentasi seperti Chungkook-jang dan tempe. Meskipun enzim ini telah dikarakterisasi dari berbagai sumber yang berbeda, enzim fibrinolitik mikroba dianggap paling menarik karena fitur-fiturnya, seperti spesifisitas meningkat, biaya produksi yang rendah, hasilnya relatif tinggi, dan kemungkinan untuk dimodifikasi secara genetik dengan teknologi DNA rekombinan dan pendekatan rekayasa protein.
Baru-baru ini, enzim fibrinolitik mikroba, karena fitur spesifiknya telah mendapatkan perhatian lebih daripada agen trombolitik konvensional untuk pengobatan trombosis. Namun, masih sedikit laporan mengenai enzim fibrinolitik yang diproduksi dari mikroorganisme laut [3]. Mikroorganisme laut termasuk bakteri dan mikroalga memiliki kemampuan yang signifikan untuk menghasilkan enzim fibrinolitik dengan sifat farmakologis yang lebih baik dan efek samping yang lebih rendah dan, karenanya, dianggap sebagai kandidat prospektif untuk produksi enzim ini dalam skala besar [1].
Berdasarkan caranya, produksi enzim fibrinolitik dari mikroba laut dapat dibagi menjadi dua, yaitu sebagai berikut:
1. Konstruksi strain rekayasa genetika
Kloning gen, mutagenesis dan teknologi DNA rekombinan telah digunakan untuk menimbulkan ekspresi berlebih (overexpression) gen penyandi enzim fibrinolitik dalam inang bakteri dan untuk merekayasa sifat katalitiknya. Dari studi yang pernah dilakukan, dapat disimpulkan bahwa kombinasi antara optimasi media kultur dan teknologi DNA rekombinan merupakan hal yang penting untuk meningkatkan titer enzim secara efektif. Berikut adalah contoh studi yang telah dilakukan untuk mengonstruksi strain rekayasa genetika mikroba laut dalam memproduksi enzim fibrinolitik:
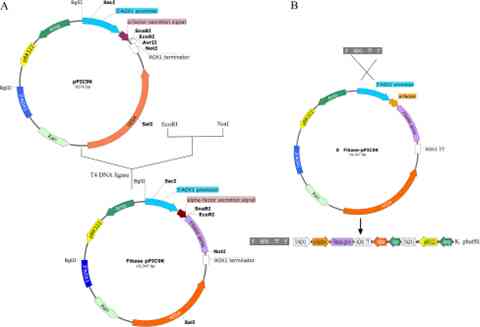
a. Yao dan rekan (2018) [4] melakukan isolasi strain Bacillus, BS15 dari makanan laut fermentasi Korea. BS15 ini diidentifikasi sebagai Bacillus pumilus. Ketika supernatan kultur bakteri tersebut dianalisis dengan sodium dodecyl sulfate polyacrylamide gel electrophoresis (SDS-PAGE) dan fibrin zymography, diketahui bahwa protein 27kDa yang dihasilkan oleh BS15 memiliki aktivitas fibrinolitik.
Gen penyandi enzim fibrinolitik dari BS15 ini, yaitu aprEBS15 dikloning ke dalam vektor Bacillus-E. coli (pHY300PLK). Gen aprEBS15 ternyata diekspresikan berlebih di dalam E. coli BL21 (B. subtilis). Hasilnya adalah enzim rekombinan (AprEBS15) yang telah dipurifikasi memiliki aktivitas fibrinolitik yang jauh lebih tinggi pada pH 8.0 dan suhu 40 degC dibandingkan enzim fibrinolitik dari B. pumilus BS15 itu sendiri.
b. Che dan rekan (2020) [3] menggunakan ragi (yeast) sebagai sistem ekspresi gen penyandi enzim fibrinolitik. Ekspresi gen protein asing yang berlebih pada ragi tidak seperti pada E. coli yang membentuk badan inklusi sehingga protein menjadi tidak aktif. Demikian pula pada B. subtilis, meskipun memberi keuntungan dalam hal sekresinya yang cepat dan ekspresinya yang lebih baik daripada E. coli, tetapi B. subtilis juga memiliki ekspresi protease yang tinggi sehingga dapat mendegradasi enzim fibrinolitik yang dihasilkannya.
Oleh karena itu, Komagataella phaffii (Pichia pastoris) sangat cocok untuk digunakan dalam produksi industri enzim fibrinolitik skala besar di samping pertumbuhannya yang cepat, keamanan mikrobiologis dan kemampuan untuk fermentasi kepadatan tinggi dalam media sederhana membuat ragi banyak dipakai secara luas dalam produk farmasi dan bioteknologi. Pada studi ini, Che dan rekan menggunakan dosis gen (meningkatkan jumlah kopi gen), optimasi kodon dan optimasi proses untuk mencapai ekspresi tinggi dan sekresi enzim fibrinolitik yang diisolasi dari B. subtilis laut.
Total 168 kodon dari gen enzim fibrinolitik B. subtilis D21 diganti dengan kodon yang disukai K. phaffii. Hasilnya menunjukkan bahwa strategi yang dikembangkan dalam studi ini dapat digunakan juga untuk meningkatkan ekspresi protein terapeutik lain yang sulit diekspresikan.
2. Pendekatan fermentasi
Dalam hal produksi enzim di sektor industri, biaya produksi menjadi salah satu faktor yang menantang. Setiap industri pasti mengharapkan hasil produksi yang tinggi dengan biaya serendah mungkin. Untuk mencapai hal ini, maka pendekatan fermentasi menjadi opsi menarik untuk diterapkan dalam memproduksi enzim fibrinolitik dengan hasil tinggi dan cara yang efisien [1]. Berikut adalah contoh studi yang telah dilakukan untuk memproduksi enzim fibrinolitik dengan pendekatan fermentasi:
a. Anusree, dkk (2020) [5] menggunakan fermentasi terendam (submerged fermentation), yaitu salah satu metode fermentasi dengan menggunakan substrat cair. Metode tersebut dioptimasi dengan waktu inkubasi 48 jam; ukuran inokulum 0,8% v/v; pH 6,0; suhu 30 degC, dan konsentrasi sumber nutrisi seperti maltosa 1,5% w/v; ekstrak ragi 1,5% w/v, NaCl 1,5% w/v dan susu bubuk skim 0,15% w/v.
Dengan metode yang telah dioptimasi tersebut, mereka berhasil meningkatkan ekspresi gen penyandi enzim fibrinolitik dari bakteri Serratia rubidaea KUAS001 (bakteri laut). Aktivitas enzim fibrinolitik yang diperoleh menjadi 2,57 kali lebih tinggi dibandingkan kondisi yang tidak dioptimasi.
b. Pan, dkk (2019) [6] menunjukkan pemanfaatan fermentasi terendam nonsteril yang mampu mengurangi biaya produksi enzim fibrinolitik dari Bacillus subtilis D21-8 hingga 24%. Produktivitas enzim juga lebih tinggi dibandingkan dengan medium steril.
c. Beberapa peneliti juga menunjukkan bahwa penggunaan dan penerapan instrumen statistika yang beragam dapat menjadi pendekatan yang berguna untuk mengoptimalkan parameter fisiko-kimia dalam memproduksi enzim fibrinolitik, seperti desain Box--Behnken [7], rancangan faktorial lengkap dua-level & metodologi permukaan respons [8], rancangan Plackett--Burman & uji satu faktor [9], metode larik ortogonal L18 [10], dan rancangan komposit pusat [11].
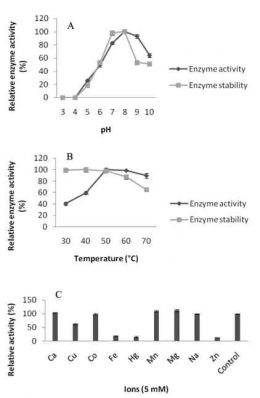
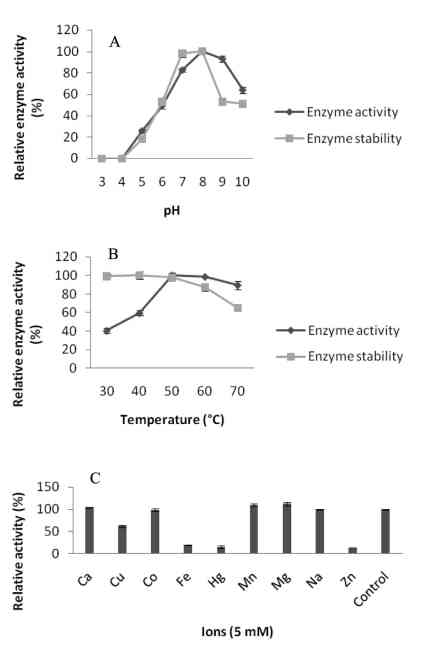
d. Farraj dan rekan (2020) [8], menerapkan rancangan faktorial lengkap dua-level & metodologi permukaan respons, mampu meningkatkan ekspresi gen penyandi enzim fibrinolitik yang diisolasi dari Bacillus flexus menggunakan proses fermentasi keadaan padat pada kondisi optimum pH 8,0 dan suhu 60 degC (lihat Gambar 2).
Studi ini juga menunjukkan bahwa Mg2+ adalah salah satu ion signifikan yang meningkatkan aktivitas enzim fibrinolitik yang juga dapat meningkatkan produksi enzim. Sedangkan Zn2+, Fe2+, dan Hg2+ menghambat aktivitas enzim secara drastis. Dengan media yang dioptimasi dan rancangan eksperimen tersebut, diperoleh produksi enzim fibrinolitik 3,5 kali lebih tinggi dibandingkan pada media yang tidak dioptimasi.
Enzim fibrinolitik yang bersumber dari mikroba laut memiliki potensi terapeutik yang sangat besar untuk mencegah dan mengobati penyakit kardiovaskular. Sayangnya, sumber baru ini masih belum banyak dieksplorasi. Karena itu, studi mengenai optimasi parameter produksi masih terus dilakukan guna menghasilkan produksi enzim yang ekonomis, efektif, dan aman sehingga dapat menjadi agen fibrinolitik yang menguntungkan dan aman di masa depan.
Oleh: Santi Tan & Btari Gavrilla Larasati
Referensi:
- Barzkar N, Jahromi ST, Vianello F. Marine microbial fibrinolytic enzymes: an overview of source, production, biochemical properties and thrombolytic activity. Marine Drugs. 2022;20(1):46. doi:10.3390/md20010046
- Kumar SS, Sabu A. Fibrinolytic enzymes for thrombolytic therapy. In: Labrou N, ed. Therapeutic enzymes: function and clinical implications. Vol 1148. Advances in Experimental Medicine and Biology. Springer Singapore; 2019:345-381. doi:10.1007/978-981-13-7709-9_15
- Che Z, Cao X, Chen G, Liang Z. An effective combination of codon optimization, gene dosage, and process optimization for high-level production of fibrinolytic enzyme in Komagataella phaffii (Pichia pastoris). BMC Biotechnol. 2020;20(1):63. doi:10.1186/s12896-020-00654-7
- Yao Z, Kim JA, Kim JH. Gene cloning, expression, and properties of a fibrinolytic enzyme secreted by Bacillus pumilus BS15 isolated from gul (oyster) jeotgal. Biotechnol Bioproc E. 2018;23(3):293-301. doi:10.1007/s12257-018-0029-7
- Anusree M, Swapna K, Aguilar CN, Sabu A. Optimization of process parameters for the enhanced production of fibrinolytic enzyme by a newly isolated marine bacterium. Bioresource Technology Reports. 2020;11:100436. doi:10.1016/j.biteb.2020.100436
- Pan S, Chen G, Wu R, Cao X, Liang Z. Non-sterile submerged fermentation of fibrinolytic enzyme by marine Bacillus subtilis harboring antibacterial activity with starvation strategy. Front Microbiol. 2019;10:1025. doi:10.3389/fmicb.2019.01025
- Kumar SS, Haridas M, Sabu A. Process optimization for production of a fibrinolytic enzyme from newly isolated marine bacterium Pseudomonas aeruginosa KU1. Biocatalysis and Agricultural Biotechnology. 2018;14:33-39. doi:10.1016/j.bcab.2018.02.001
- Al Farraj DA, Kumar TSJ, Vijayaraghavan P, et al. Enhanced production, purification and biochemical characterization of therapeutic potential fibrinolytic enzyme from a new Bacillus flexus from marine environment. Journal of King Saud University - Science. 2020;32(7):3174-3180. doi:10.1016/j.jksus.2020.09.004
- Krishnamurthy A, Belur P, Rai P, Rekha P. Production of fibrinolytic enzyme by the marine isolate Serratia marcescens subsp. sakuensis and its In-vitro anticoagulant and thrombolytic potential. J PURE APPL MICROBIO. 2017;11(4):1987-1998. doi:10.22207/JPAM.11.4.41
- Mahajan PM, Nayak S, Lele SS. Fibrinolytic enzyme from newly isolated marine bacterium Bacillus subtilis ICTF-1: media optimization, purification and characterization. Journal of Bioscience and Bioengineering. 2012;113(3):307-314. doi:10.1016/j.jbiosc.2011.10.023
- Pablo Eugenio da Costa e S, Fabiana America Silva Dantas de S, Rafaela Cavalcante de B, Daniela Araujo Viana M, Ana Lucia Figueiredo P, Raquel Pedrosa B. Enhanced production of fibrinolytic protease from microalgae Chlorella vulgaris using glycerol and corn steep liquor as nutrient. Ann Microbiol Res. 2017;1(1). doi:10.36959/958/564